Structural search and advanced query search is temporarily unavailable. We are working to fix this issue. Thank you for your support and patience.
Dehydroglycine (M2MDB001730)
| Record Information | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Version | 2.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Creation Date | 2012-07-30 14:55:19 -0600 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Update Date | 2015-06-03 17:21:10 -0600 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Secondary Accession Numbers |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identification | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name: | Dehydroglycine | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description | Dehydroglycine is a member of the chemical class known as Alpha Amino Acids and Derivatives. These are amino acids in which the amino group is attached to the carbon atom immediately adjacent to the carboxylate group (alpha carbon).Dehydroglycine is catalyzed by ThiH. ThiH is a tyrosine lyase that cleaves the C alpha-C beta bond of tyrosine, generating p-cresol as a by-product, to form dehydroglycine. (PMID 19923213) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
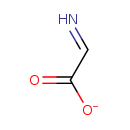
| Structure | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyms: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Formula: | C2H2NO2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weight: | Average: 72.0428 Monoisotopic: 72.008553313 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI Key: | TVMUHOAONWHJBV-UHFFFAOYSA-M | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI: | InChI=1S/C2H3NO2/c3-1-2(4)5/h1,3H,(H,4,5)/p-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS number: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IUPAC Name: | 2-iminoacetate | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Traditional IUPAC Name: | 2-iminoacetate | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILES: | [O-]C(=O)C=N | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Taxonomy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description | belongs to the class of organic compounds known as carboxylic acids. Carboxylic acids are compounds containing a carboxylic acid group with the formula -C(=O)OH. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kingdom | Organic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Super Class | Organic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Class | Carboxylic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sub Class | Carboxylic acids | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Direct Parent | Carboxylic acids | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Alternative Parents | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Substituents |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molecular Framework | Aliphatic acyclic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Descriptors |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| State: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Charge: | -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Experimental Properties: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Predicted Properties |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Biological Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cellular Locations: | Cytoplasm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reactions: | Adenosine triphosphate + Dehydroglycine + 1-Deoxy-D-xylulose 5-phosphate + Hydrogen ion + IscS with bound sulfur + NADPH > 4-Methyl-5-(2-phosphoethyl)-thiazole + Adenosine monophosphate + Carbon dioxide +2 Water + IscS sulfur acceptor protein + NADP + Pyrophosphate S-Adenosylmethionine + NADPH + L-Tyrosine > p-Cresol + 5'-Deoxyadenosine + Dehydroglycine + Hydrogen ion + L-Methionine + NADP Dehydroglycine + Water > Glyoxylic acid + Ammonia L-Tyrosine + S-Adenosylmethionine + a reduced electron acceptor > Dehydroglycine + p-Cresol + 5'-Deoxyadenosine + L-Methionine + an oxidized electron acceptor + Hydrogen ion 1-Deoxy-D-xylulose 5-phosphate + Dehydroglycine + a thiocarboxy-[ThiS-Protein] > 2-((2R,5Z)-2-Carboxy-4-methylthiazol-5(2H)-ylidene)ethyl phosphate + a ThiS sulfur-carrier protein +2 Water L-Tyrosine + S-adenosyl-L-methionine + NADPH > Dehydroglycine + 4-Methylcatechol + 5'-Deoxyadenosine + L-Methionine + NADP + Hydrogen ion | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMPDB Pathways: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| KEGG Pathways: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EcoCyc Pathways: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Concentrations | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Not Available | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synthesis Reference: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Material Safety Data Sheet (MSDS) | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Links | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Links: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Enzymes
- General function:
- Involved in metabolic process
- Specific function:
- Catalyzes the removal of elemental sulfur and selenium atoms from cysteine and selenocysteine to produce alanine. Functions as a sulfur delivery protein for NAD, biotin and Fe-S cluster synthesis. Transfers sulfur on 'Cys-456' of thiI in a transpersulfidation reaction. Transfers sulfur on 'Cys-19' of tusA in a transpersulfidation reaction. Functions also as a selenium delivery protein in the pathway for the biosynthesis of selenophosphate
- Gene Name:
- iscS
- Uniprot ID:
- P0A6B7
- Molecular weight:
- 45089
Reactions
| L-cysteine + acceptor = L-alanine + S-sulfanyl-acceptor. |
- General function:
- Involved in nucleotide binding
- Specific function:
- Catalyzes the adenylation by ATP of the carboxyl group of the C-terminal glycine of sulfur carrier protein ThiS
- Gene Name:
- thiF
- Uniprot ID:
- P30138
- Molecular weight:
- 26970
Reactions
| ATP + [ThiS] = diphosphate + adenylyl-[ThiS]. |
- General function:
- Involved in RNA binding
- Specific function:
- Catalyzes the ATP-dependent transfer of a sulfur to tRNA to produce 4-thiouridine in position 8 of tRNAs, which functions as a near-UV photosensor. Also catalyzes the transfer of sulfur to the sulfur carrier protein ThiS, forming ThiS-thiocarboxylate. This is a step in the synthesis of thiazole, in the thiamine biosynthesis pathway. The sulfur is donated as persulfide by iscS
- Gene Name:
- thiI
- Uniprot ID:
- P77718
- Molecular weight:
- 54973
Reactions
| L-cysteine + 'activated' tRNA = L-serine + tRNA containing a thionucleotide. |
| [IscS]-SSH + [ThiS]-COAMP = [IscS]-SH + [ThiS]-COSH + AMP. |
- General function:
- Involved in catalytic activity
- Specific function:
- Catalyzes the rearrangement of 1-deoxy-D-xylulose 5- phosphate (DXP) to produce the thiazole phosphate moiety of thiamine. Sulfur is provided by the thiocarboxylate moiety of the carrier protein ThiS. In vitro, sulfur can be provided by H(2)S
- Gene Name:
- thiG
- Uniprot ID:
- P30139
- Molecular weight:
- 26896
Reactions
| 1-deoxy-D-xylulose 5-phosphate + 2-iminoacetate + thiocarboxy-adenylate-[sulfur-carrier protein ThiS] = 2-((2R,5Z)-2-carboxy-4-methylthiazol-5(2H)-ylidene)ethyl phosphate + [sulfur-carrier protein ThiS] + 2 H(2)O. |
- General function:
- Coenzyme transport and metabolism
- Specific function:
- Is the sulfur donor in the synthesis of the thiazole phosphate moiety of thiamine phosphate
- Gene Name:
- thiS
- Uniprot ID:
- O32583
- Molecular weight:
- 7311
- General function:
- Involved in catalytic activity
- Specific function:
- Catalyzes the radical-mediated cleavage of tyrosine to dehydroglycine and p-cresol
- Gene Name:
- thiH
- Uniprot ID:
- P30140
- Molecular weight:
- 43320
Reactions
| L-tyrosine + S-adenosyl-L-methionine + reduced acceptor = 2-iminoacetate + 4-methylphenol + 5'-deoxyadenosine + L-methionine + acceptor + 2 H(+). |