Structural search and advanced query search is temporarily unavailable. We are working to fix this issue. Thank you for your support and patience.
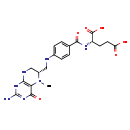
5-Methyltetrahydrofolic acid (M2MDB000368)
| Record Information | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Version | 2.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Creation Date | 2012-05-31 13:51:35 -0600 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Update Date | 2015-09-17 15:41:11 -0600 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Secondary Accession Numbers |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identification | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name: | 5-Methyltetrahydrofolic acid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description | 5 methyltetrahydrofolic acid (5-MTHF) is the most biologically active form of the B-vitamin folic acid, also known generically as folate. It is a methylated derivate of tetrahydrofolate (THF, H4F). It is generated by methylenetetrahydrofolate reductase (MTHFR) from 5,10-methylenetetrahydrofolate (5,10-CH2-THF, MTHF) and used to recycle homocysteine back to methionine by 5-methyltetrahydrofolate-homocysteine methyltransferase (MTR) or methionine synthase (MS). 5-MTHF functions, in concert with vitamin B12, as a methyl-group donor involved in the conversion of the amino acid homocysteine to methionine. Methyl (CH3) group donation is vital to many cellular processes. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structure | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyms: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Formula: | C20H25N7O6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weight: | Average: 459.4558 Monoisotopic: 459.186631567 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI Key: | ZNOVTXRBGFNYRX-ZGTCLIOFSA-N | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI: | InChI=1S/C20H25N7O6/c1-27-12(9-23-16-15(27)18(31)26-20(21)25-16)8-22-11-4-2-10(3-5-11)17(30)24-13(19(32)33)6-7-14(28)29/h2-5,12-13,22H,6-9H2,1H3,(H,24,30)(H,28,29)(H,32,33)(H4,21,23,25,26,31)/t12?,13-/m1/s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS number: | 134-35-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IUPAC Name: | (2S)-2-{[4-({[(6S)-2-amino-5-methyl-4-oxo-1,4,5,6,7,8-hexahydropteridin-6-yl]methyl}amino)phenyl]formamido}pentanedioic acid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Traditional IUPAC Name: | 5-methyltetrahydrofolate | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILES: | CN1C(CNC2=CC=C(C=C2)C(=O)N[C@H](CCC(O)=O)C(O)=O)CNC2=C1C(=O)NC(N)=N2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Taxonomy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description | belongs to the class of organic compounds known as n-acyl-l-alpha-amino acids. These are n-acylated alpha amino acids which have the L-configuration of the alpha-carbon atom. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kingdom | Organic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Super Class | Organic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Class | Carboxylic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sub Class | Amino acids, peptides, and analogues | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Direct Parent | N-acyl-L-alpha-amino acids | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Alternative Parents |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Substituents |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molecular Framework | Aliphatic acyclic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Descriptors |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| State: | Solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Charge: | -2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Experimental Properties: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Predicted Properties |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Biological Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cellular Locations: | Cytoplasm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reactions: | 5-Methyltetrahydrofolic acid + L-Homocysteine <> Hydrogen ion + L-Methionine + Tetrahydrofolic acid 2 Hydrogen ion + 5,10-Methylene-THF + NADH > 5-Methyltetrahydrofolic acid + NAD 5-Methyltetrahydrofolic acid + L-Homocysteine <> Tetrahydrofolic acid + L-Methionine 5-Methyltetrahydrofolic acid + NADP <> 5,10-Methylene-THF + NADPH + Hydrogen ion 5-Methyltetrahydrofolic acid + NAD <> 5,10-Methylene-THF + NADH + Hydrogen ion L-Homocysteine + 5-Methyltetrahydrofolic acid L-Methionine + Tetrahydrofolic acid 5-Methyltetrahydrofolic acid + NAD(P)(+) > 5,10-Methylene-THF + NAD(P)H 5-Methyltetrahydrofolic acid + L-Homocysteine > Tetrahydrofolic acid + L-Methionine 5-Methyltetrahydrofolic acid + NAD + NADP <> 5,10-Methylene-THF + NADH + NADPH + Hydrogen ion 5,10-Methylene-THF + NADPH + Hydrogen ion + 5,10-Methylene-THF + NADPH > 5-Methyltetrahydrofolic acid + NADP + 5-Methyltetrahydrofolic acid 5-Methyltetrahydrofolic acid + Homocysteine + 5-Methyltetrahydrofolic acid + Homocysteine > Tetrahydrofolic acid + L-Methionine + Tetrahydrofolic acid 2 Hydrogen ion + 5 5,10-Methylene-THF + NADH >5 5-Methyltetrahydrofolic acid + NAD 5 5-Methyltetrahydrofolic acid + L-Homocysteine <> Hydrogen ion + L-Methionine + Tetrahydrofolic acid 2 Hydrogen ion + 5 5,10-Methylene-THF + NADH >5 5-Methyltetrahydrofolic acid + NAD 5 5-Methyltetrahydrofolic acid + L-Homocysteine <> Hydrogen ion + L-Methionine + Tetrahydrofolic acid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMPDB Pathways: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| KEGG Pathways: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EcoCyc Pathways: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Concentrations | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Not Available | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synthesis Reference: | Gennari, Federico. Process for producing 5-methyltetrahydrofolic acid and its salts. U.S. (1992), 6 pp. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Material Safety Data Sheet (MSDS) | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Links | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Links: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Enzymes
- General function:
- Involved in methylenetetrahydrofolate reductase (NADPH) activity
- Specific function:
- 5-methyltetrahydrofolate + NAD(P)(+) = 5,10- methylenetetrahydrofolate + NAD(P)H
- Gene Name:
- metF
- Uniprot ID:
- P0AEZ1
- Molecular weight:
- 33102
Reactions
| 5-methyltetrahydrofolate + NAD(P)(+) = 5,10-methylenetetrahydrofolate + NAD(P)H. |
- General function:
- Involved in methionine synthase activity
- Specific function:
- Catalyzes the transfer of a methyl group from methyl- cobalamin to homocysteine, yielding enzyme-bound cob(I)alamin and methionine. Subsequently, remethylates the cofactor using methyltetrahydrofolate
- Gene Name:
- metH
- Uniprot ID:
- P13009
- Molecular weight:
- 135996
Reactions
| 5-methyltetrahydrofolate + L-homocysteine = tetrahydrofolate + L-methionine. |
- General function:
- Involved in 5-methyltetrahydropteroyltriglutamate-homocysteine S-methyltransferase activity
- Specific function:
- Catalyzes the transfer of a methyl group from 5- methyltetrahydrofolate to homocysteine resulting in methionine formation
- Gene Name:
- metE
- Uniprot ID:
- P25665
- Molecular weight:
- 84673
Reactions
| 5-methyltetrahydropteroyltri-L-glutamate + L-homocysteine = tetrahydropteroyltri-L-glutamate + L-methionine. |