Structural search and advanced query search is temporarily unavailable. We are working to fix this issue. Thank you for your support and patience.
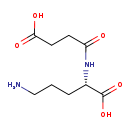
N2-Succinyl-L-ornithine (M2MDB000295)
| Record Information | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Version | 2.0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Creation Date | 2012-05-31 13:47:30 -0600 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Update Date | 2015-06-03 15:53:50 -0600 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Secondary Accession Numbers |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identification | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name: | N2-Succinyl-L-ornithine | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description | N2-Succinyl-L-ornithine is a substrate for Ornithine aminotransferase (mitochondrial). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structure | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyms: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Formula: | C9H16N2O5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Weight: | Average: 232.2337 Monoisotopic: 232.105921632 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI Key: | VWXQFHJBQHTHMK-LURJTMIESA-N | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI: | InChI=1S/C9H16N2O5/c10-5-1-2-6(9(15)16)11-7(12)3-4-8(13)14/h6H,1-5,10H2,(H,11,12)(H,13,14)(H,15,16)/t6-/m0/s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS number: | 899816-95-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IUPAC Name: | (2S)-5-amino-2-(3-carboxypropanamido)pentanoic acid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Traditional IUPAC Name: | N(2)-succinyl-L-ornithine | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMILES: | NCCC[C@H](NC(=O)CCC(O)=O)C(O)=O | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemical Taxonomy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Description | belongs to the class of organic compounds known as n-acyl-alpha amino acids. N-acyl-alpha amino acids are compounds containing an alpha amino acid which bears an acyl group at its terminal nitrogen atom. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kingdom | Organic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Super Class | Organic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Class | Carboxylic acids and derivatives | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sub Class | Amino acids, peptides, and analogues | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Direct Parent | N-acyl-alpha amino acids | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Alternative Parents | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Substituents |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molecular Framework | Aliphatic acyclic compounds | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Descriptors |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physical Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| State: | Solid | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Charge: | -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Melting point: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Experimental Properties: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Predicted Properties |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Biological Properties | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cellular Locations: | Cytoplasm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reactions: | 2 Hydrogen ion + 2 Water + N2-Succinyl-L-arginine > Carbon dioxide +2 Ammonium + N2-Succinyl-L-ornithine alpha-Ketoglutarate + N2-Succinyl-L-ornithine <> L-Glutamate + N2-Succinyl-L-glutamic acid 5-semialdehyde N2-Succinyl-L-arginine + 2 Water <> N2-Succinyl-L-ornithine + Carbon dioxide +2 Ammonia N2-Succinyl-L-arginine + Water > N2-Succinyl-L-ornithine + Ammonia + Carbon dioxide N2-Succinyl-L-ornithine + Oxoglutaric acid > N2-Succinyl-L-glutamic acid 5-semialdehyde + L-Glutamate N2-Succinyl-L-arginine + 2 Water > N2-Succinyl-L-ornithine +2 Ammonia + Carbon dioxide N2-succinyl-L-arginine + 2 Water + 2 Hydrogen ion + N2-succinyl-L-arginine > Carbon dioxide +2 Ammonium + N2-Succinyl-L-ornithine N2-Succinyl-L-ornithine + Oxoglutaric acid > L-Glutamic acid + N2-Succinyl-L-glutamic acid 5-semialdehyde + L-Glutamate N2-Succinyl-L-arginine + 2 Water <> N2-Succinyl-L-ornithine + Carbon dioxide +2 Ammonia N2-Succinyl-L-arginine + 2 Water <> N2-Succinyl-L-ornithine + Carbon dioxide +2 Ammonia | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SMPDB Pathways: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| KEGG Pathways: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EcoCyc Pathways: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Concentrations | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Not Available | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spectra: | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| References: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synthesis Reference: | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Material Safety Data Sheet (MSDS) | Not Available | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Links | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| External Links: |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Enzymes
- General function:
- Involved in N-succinylarginine dihydrolase activity
- Specific function:
- Catalyzes the hydrolysis of N(2)-succinylarginine into N(2)-succinylornithine, ammonia and CO(2)
- Gene Name:
- astB
- Uniprot ID:
- P76216
- Molecular weight:
- 49298
Reactions
| N(2)-succinyl-L-arginine + 2 H(2)O = N(2)-succinyl-L-ornithine + 2 NH(3) + CO(2). |
- General function:
- Involved in transaminase activity
- Specific function:
- Catalyzes the transamination of N(2)-succinylornithine and alpha-ketoglutarate into N(2)-succinylglutamate semialdehyde and glutamate. Can also act as an acetylornithine aminotransferase
- Gene Name:
- astC
- Uniprot ID:
- P77581
- Molecular weight:
- 43665
Reactions
| N(2)-succinyl-L-ornithine + 2-oxoglutarate = N-succinyl-L-glutamate 5-semialdehyde + L-glutamate. |